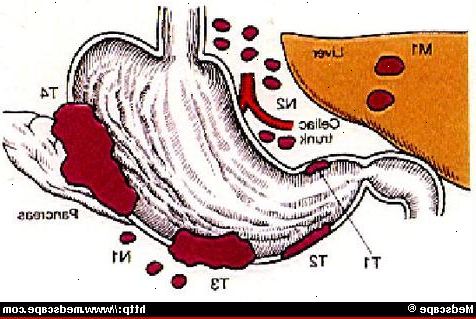
Hva er gastrointestinal kreft?
Spiserørskreft står for om lag 3 prosent av kreftdødsfall.
Magesekken går fra munn til anus, og omfatter spiserøret (spiserøret), mage, tynntarm, tarm-eller tarmen, og i tykktarmen (colon og rektum).
Kreft kan påvirke enhver del av mage-tarmkanalen, men merkelig nok, er det sjelden i tynntarmen hvor det meste fordøyelsen foregår.
- Tarmkreft (kolorektal) er den nest vanligste årsaken til kreft-dødsfall (etter lungekreft ), påvirker seks prosent av befolkningen i Westernised (industrialiserte) land og forårsaker død i om lag 3 prosent. Om lag 25 prosent av alle dødsfall er forårsaket av kreft i industrialiserte land, og tarmkreft står for 12,5 prosent av disse dødsfallene.
- Mage kreft står for om lag 8 prosent av kreft dødsfall og forekommer i dobbelt så mange menn som kvinner. Det er gradvis blitt mindre vanlig, men, dessverre, har denne høsten blitt balansert ved en økning i kreft i spiserøret (spesielt en kjertel typen som kalles adenokarsinom) hos menn. Dette er den syvende vanligste kreftformen.
- Spiserørskreft står for om lag 3 prosent av kreft dødsfall og forholdet mellom berørte menn til kvinner er 1.8:1. Europe menn nå har den nest høyeste satsen i Europa, etter at franske menn.
- Kreft i bukspyttkjertelen står for om lag 4 prosent av kreft dødsfall og rammer begge kjønn omtrent likt. En tredjedel av alle tilfellene oppstår hos de under 65 år.
- Kreft som utvikler først i leveren (primær leverkreft) er sterkt knyttet med hepatitt virus infeksjon. Det er uvanlig i vestlige land der frekvensen av hepatitt er relativt lav, men ofte er den vanligste årsaken til kreft-dødsfall i utviklingsland der hepatitt er mye hyppigere. Samlet det står for bare om lag 0,7 prosent av kreftdødsfall i vestlige land. Imidlertid er leveren et felles område for andre gastrointestinal kreft til å spre seg, særlig kolorektal kreft, noe som resulterer i såkalte sekundære avsetninger eller metastatisk kreft.
Hvordan reduserer jeg min risiko for disse kreftformene?
Flere endringer i livsstil kan redusere risikoen for å få gastrointestinal kreft.
Drikk alkohol med måte
Et høyt alkoholinntak er assosiert med økt risiko for kreft i:
- spiserøret - spesielt plateepitel kreft der alkoholholdige brennevin og røyking synes å ha additive effekter.
- bukspyttkjertelen - hvis høyt alkoholinntak i utgangspunktet fører til kronisk betennelse eller pankreatitt, som innebærer en økt risiko for kreft i bukspyttkjertelen.
- leveren - hvis høyt alkoholinntak fører til skrumplever, skade på grunn av kronisk betennelse som er en viktig risikofaktor for primær leverkreft.
- tarmen.
Unngå røyking
Røyking dobler risikoen for kreft i bukspyttkjertel og er, særlig når alkoholholdige ånder er også full, forbundet med økt risiko for kreft i spiserøret.
Spis rikelig med grønne grønnsaker
Et høyt inntak av grønne grønnsaker er forbundet med en redusert risiko for tarmkreft og en høy vitamin C inntak (funnet i frukt og grønne grønnsaker) er forbundet med redusert risiko for magekreft.
Unngå bevart eller brent kjøtt
Saltet og røkt kjøtt er forbundet med høy risiko for magekreft, sannsynligvis på grunn av sitt høye innhold av nitrater som på magen skjema sterkt kreftfremkallende nitrosogrupper-aminer.
Brent kjøtt har vist seg å ha sammenheng med tarmkreft på grunn av deres høye innhold av kreftfremkallende cykliske aminer. Et høyt inntak av rødt og bearbeidet kjøtt er spesielt forbundet med økt risiko for tarmkreft.
Holde en normal vekt
Fedme innebærer en økt risiko for tarmkreft blant menn. Fedme øker også risikoen for diabetes som selv er knyttet til et beskjedent økt risiko for kreft i bukspyttkjertelen.
Ta regelmessig mosjon
Vanlig fysisk aktivitet er forbundet med en redusert risiko for tarmkreft, uavhengig av kroppsvekten.
Kan screening tester oppdage gastrointestinal kreft før de forårsaker symptomer?
Screening er prosessen med å sjekke folk som ikke har noen symptomer for uventet sykdom, som deretter kan behandles mer vellykket enn hvis sykdommen hadde stått inntil det viste seg.
Screeningprogrammer er allerede på plass for brystkreft og livmorhalskreft hos kvinner. HNFA tarmkreft Screening Programme (BCSP) startet i 2006 og har blitt rullet ut til alle fire nasjoner foretatt hvert 2. år for pasienter registrert med en GP.
Hver kreft må vurderes separat, men noen screeningprogrammet bør ha visse felles egenskaper som er avgjørende for suksess:
- sykdommen bør være ganske vanlig i befolkningen eller en gruppe mennesker som anses å trenge screening (ellers fordel til ett individ ikke vil være tilstrekkelig til å oppveie risikoen og ulempene ved screening til resten).
- en diagnostisk test for å detektere tilstanden er nødvendig som er enkel, billig og pålitelig.
- effektiv behandling bør eksistere.
Den siste av disse egenskapene kan virke grei - sikkert kirurgi er effektiv behandling for alle gastrointestinal kreft hvis de er fanget tidlig?
Selv om dette er en rimelig generalisering dette utsagnet er ikke sant i alle tilfeller. Mange kreftformer skur lite antall celler eller 'micrometastases' i blod eller lymfe kanaler fra et svært tidlig stadium slik at fjerning av den opprinnelige (primær) kreft ikke kan kurere pasienten. I disse tilfeller virker kroppens eget immunforsvar mot disse tumorceller minst like viktig som den hastighet med hvilken den primære kreft er identifisert og fjernet.
Screening for tarmen (tykk) kreft
Dette kreft er den beste "bet" for å få en vellykket screeningprogram av flere grunner: det er relativt vanlig, kurere priser for kirurgi er svært høy (> 90 prosent) hvis den er fanget på et tidlig stadium, og i de fleste tilfeller en pre -kreft stadium kalles en polypp kan bli funnet og slett fjernet for å forebygge kreft utvikler seg.
Befolkning screening tester
Identifiseringen av en enkel test er mindre grei. Den enkleste testen er blod i avføringen screening (se etter blod i avføringen som ikke er synlig) selv om dette innebærer å samle avføring, noe som er ubehagelig. Men hovedproblemet er unøyaktighet av testen.
En positiv fekal okkult blod test viser omtrent en 10 prosent sjanse for kreft eller en 34 prosent sjanse for en polypp, men testen vil være negativ for opp til 50 prosent av krefttilfellene (dette tallet faller til om lag 30 prosent dersom testen gjentas tre dager på rad).
En positiv test må bli etterfulgt av koloskopi (en undersøkelse av tarmen med et tynt teleskop). Så, betyr den høye hastigheten som blod i avføringen er funnet når kreften ikke er tilstede (falsk-positiv rate) at betydelig stress er forårsaket til personer som senere viser seg å ha en sunn kolon. Men andre diagnose blir funnet, for eksempel divertikkelsykdom, hemoroider eller IBD. Det er også god mulighet for en helse forbedring melding som skal diskuteres med pasienten
Rapporter om de beste resultatene viser at dersom årlig blod i avføringen testing anbefales til alle personer over 50 år, ville screening reduserer dødeligheten av kolorektal kreft med om lag en tredjedel. Dette resultatet høres vel verdt og så dette screening-programmet er nå anbefalt som standard praksis i Europa. Det koster omtrent US $ 45 000 for å få ett år av livet - et tall sannsynlig å være utenfor rekkevidde for de fleste offentlige helsevesen.
Dessuten vil kun om lag 3 prosent av befolkningen (unntatt høy-risiko individer) dør av tykktarmskreft, og de vil bli diagnostisert på en gjennomsnittsalder på 65 år med omtrent en 10-års levetid. Så fikk den gjennomsnittlige lengden på livet per person dersom alle dødsfall fra kolorektal kreft kan forebygges ville være 3 prosent på 10 år som er fire måneder.
Hvis en tredjedel av dødsfallene ble forhindret, fikk livslengde vil beløpe seg til ca fem uker. Videre kan denne fordelen være lavere fortsatt i noen som følger en sunn livsstil med høyt grønnsak inntak og rikelig med mosjon.
Den HNFA BCSP er fullt implementert og pilotstudier av "tarm Scope 'startet i april 2013
I teorien er fleksibel sigmoidoskopi en bedre screening test fordi den har en mye bedre sjanse enn okkult blod screening for å påvise forstadier til kreft polypper. Men det har ulempene ved å være mer inngripende for pasienten og for uunngåelig mangler kreft høyere opp i tarmen som er utenfor rekkevidden av sigmoidoscope.
Dersom polypper er funnet i dette programmet da pasienten blir tilbudt en koloskopi.
Så i Europa, eksisterer trykk for å inkludere koloskopi (undersøkelse av hele tykktarmen med en fleksibel teleskop) rutinemessig som en del av en screening-programmet som også inneholder okkult blod i avføringen testing. Europas eksperter se dette forslaget som for tidlig og foreslå at rutinemessig koloskopi må bli funnet verdig i fremtidige studier før de blir introdusert for screening.
Screening for høy-risiko individer
Screening tester er mer sannsynlig å finne sykdom hos personer som har høyere risiko for sykdommen enn den generelle befolkningen. Så, vil screening av høy-risiko individer forbedre den generelle dra nytte av en screening test. To grupper er generelt ansett å trenge screening:
- personer som har en første-graders slektning (foreldre, bror, søster eller barn) som utviklet kolorektal kreft før fylte 45, hvis risiko for å utvikle kolorektal kreft i løpet av livet er en av 10.
- personer som har to (eller flere) første-graders slektninger med kolorektal kreft, som har minst en av seks levetid risiko.
Siden kolorektal kreft som går i familier (arvelig eller genetisk betinget) har en tendens til å skje ved en gjennomsnittsalder på ca 50 (Alder på 40 for FAP), potensialet livslengde fått for hver skjermet individ er mye større enn for en normal-risiko individ.
Fordelen er nok ikke helt 10 prosent av 25 år (se beregningene ovenfor) fordi enkelte kreftformer funnet vil være 'sporadisk' (oppstå ved en tilfeldighet) snarere enn genetisk bestemt, og så vil ha en eldre debutalder.
Likevel, den gjennomsnittlige fordelen per skjermet individ, forutsatt en 50 prosent reduksjon i kreft dødelighet, ville sikkert være større enn 12 måneder.
Screeningtesten må være koloskopi på grunn av tendensen av visse arvelige tykktarm kreft til å være i den høyeste delen av tykktarmen (blindtarm).
Screening bør startes ca 10 år tidligere enn den alder da den yngste berørte relative utviklet kreft og bør gjøres hvert femte år.
Arvelig non-polypose tykktarmskreft (Lynch syndrom tidligere kjent som HNPCC)
Dette er en type kolorektal kreft som går i familier og har en tendens til å forårsake kreft i relativt ung alder - under 45 år.
Flertallet av unormale gener ansvarlig for HNPCC har nå blitt identifisert, så laboratorier har begynt å tilby DNA-testing. Dette kan utføres på vev lagret fra tykktarmskreft kirurgi utført på et berørt relativ i det siste, slik at hvis en unormal gen er funnet, kan resten av familien bli tilbudt blod screening for dette genet.
Bare familiemedlemmer funnet å ha denne type mutasjon vil da trenge colonoscopic screening. Denne formen for genetisk testing er ennå ikke allment tilgjengelig i Europa.
Ett stort problem i screening pasienter med mulig HNPCC er at personer med en mutant HNPCC genet har en økt risiko ikke bare for kolorektal kreft, men også for kreft i mage, livmor, eggstokker og bryster. Dermed er det rimelig grunn til å foreslå at, en gang identifisert, bør disse personene gjennomgå regelmessig screening av alle disse organene, noe som ville innebære vanlig koloskopi, gastroskopi (teleskop undersøkelse av magen), mammografi (bryst røntgen), bekken ultralyd (ultralyd undersøkelse av bekken organer) og livmor cytologi (undersøkelse av slimhinnen i livmoren).
Dette er en stor oppgave, og om risiko og ulempe av en så kompleks screening diett er balansert fordelene er ennå ikke kjent.
Familiær polypose coli eller familiær adenomatøs polypose (FAP)
Familiær polypose coli eller familiær adenomatøs polypose (FAP) er mye sjeldnere enn HNPCC men har en tendens til å påvirke færre organer. Tilstanden gir opphav til kreft i tarmen eller tolvfingertarmen (den første delen av tynntarmen under magen) og en sjelden, men potensielt livstruende tumor kalt en desmoid som oppstår fra abdominal bindevev, som støtter og omgir indre organer.
I FAP, er tarmkreft tilnærmet ine vitable uten behandling, så det er viktig å skjerme direkte slektninger av enhver person med FAP. Utsatte individer (som ofte kan bli identifisert ved DNA-testing) trenger regelmessig fleksibel sigmoidoskopi eller koloskopi fra ca 10 år, og hvis FAP er bekreftet, vil den unge trenger deres tykktarmen fjernes kirurgisk for å unngå påfølgende kreft formasjon (profylaktisk colectomy).
Inflammatorisk tarmsykdom
Folk som enten har ulcerøs kolitt eller Crohns sykdom forårsaker kolon betennelse (kolitt) som berører mer enn halvparten av tykktarmen, har en ca 10 ganger økt risiko for tykktarmskreft.
Standarden anbefaling er at slike personer skal ha koloskopi utføres årlig når kolitt har vært til stede i åtte år.
Hovedformålet med screening er å oppdage forstadier til kreft. Med kolitt, disse oppstår som flate lesjoner som celler har en endret utseende (dysplasi) under micrscope. Ved høy klasse (alvorlig) dysplasi er funnet og bekreftet ved minst to uavhengige eksperter (fordi diagnose er vanskelig og temmelig subjektive) deretter profylaktisk colectomy er nødvendig.
Dette screeningprogrammet, men nå ganske standard i vestlige land, har vært med rette kritisert fordi det ikke har blitt studert tilstrekkelig.
I tillegg har gjennomgang av lignende programmer fra store sykehus vist at bare om lag 50 prosent av krefttilfellene som utvikler i løpet av programmet er faktisk oppdaget av colonoscopies.
Endelig er ca 200 kolonoskopier utført for hver kreft oppdages og kostnaden per leveår spart er omtrent US $ 250000 hvis koloskopi utføres årlig.
Heldigvis tyder bevis for at kreften rate i kolitt er fallende, muligens på grunn av en kreft-forebygge effekten av mesalazin, et stoff tatt for å behandle betennelse i tarmen, slik screening kan til slutt bli unødvendig.
Kreft i spiserøret
Øsofageal kreft ikke er tilstrekkelig utbredt å rettferdiggjøre bruken av screening-prosedyren med mindre den enkelte er høy risiko.
Screening for høy-risiko individer
Den screening prosedyre for høy-risiko individer er endoskopi (intern undersøkelse av spiserøret med et teleskop) og biopsi (fjerning av en liten mengde vev til undersøkelse under mikroskop).
Personer med langvarige sure oppstøt, den vanligste årsaken til "halsbrann", er i faresonen for å utvikle kreft i spiserøret hvis syre som søl opp fra magen skader slimhinnen i nedre del av spiserøret.
Normalt er fôr laget av plateepitel celler, som er svært lik hudceller. Med sure oppstøt, kan disse plateepitelceller erstattes av slim-utsondrende celler som ligner på de som finnes i tarmen. Dette cellular endringen er kjent som 'Barretts spiserør' (etter at EU-kirurgen som først beskrev den) og dessverre innebærer en økt risiko for kreft i nedre spiserør.
Det har blitt antydet at personer med Barretts øsofagus bør gjennomgå årlig endoskopi for å sjekke fôr celler for pre-ondartet forandring. I noen sykehus, laser terapi benyttes eksperimentelt for å reversere prosessen.
Ett stort problem med å planlegge en screening programmet er at omtrent en tredjedel av den voksne vestlige befolkningen har minst mindre grader av Barretts spiserør. De fleste eksperter er enige om at dersom denne endringen strekker seg over minst 5 cm i nedre spiserør deretter levetid risiko for kreft i spiserøret er trolig om lag 10 prosent og endoskopisk screening er berettiget, men hele området er fortsatt gjenstand for betydelig uenighet og endring.
Personer som røyker er spesielt utsatt for å utvikle denne typen kreft, og noen hevder at risikoen hos ikke-røykere er for lav til å rettferdiggjøre screening.
Magekreft
Magekreft er for sjelden i de fleste vestlige land for å rettferdiggjøre screening. Situasjonen er annerledes i Japan hvor mage kreft står for 11 prosent av alle dødsfall hos menn.
Screening med gastroskopi er utført på arbeidsplassen og dødsfall priser fra kreften har falt markert, men om de to er i slekt er ikke kjent.
En annen screening teknikk er barium radiologi der pasienten svelger barium væske som viser innsiden av magen på røntgen. Denne testen er lettere for pasienten, men mindre nøyaktig enn gastroskopi, og tillater ikke en biopsi for å bli tatt.
Risiko for magekreft er sterkt knyttet til mage infeksjon med Helicobacter pylori, fant en bakterie i omtrent 30 prosent av vestlige. Videre H. pylori som forårsaker kreft i magesekken i eksperimenter på dyr.
Bakterien er også antatt å forårsake duodenalsår, så utbredt testing for H. pylori etterfulgt av riktig behandling kan betydelig redusere forekomsten av både mage kreft og magesår.
Et alternativ til denne strategien som er under utvikling er en vaksine mot H. pylori. Det er imidlertid en forventet problemer med disse metodene som alvorlig H. pylori-infeksjon kan skade syre-produserende celler og hemmer magesyresekresjonen produksjon.
Utrydding av bakteriene kan da øke syre produksjon og føre til en økt forekomst av halsbrann og derfor muligens selv til en økt forekomst av kreft i spiserøret.
Det er derfor langt fra sikkert at den samlede effekten av H. pylori utrydding ville være fordelaktig. I Japan har en blodprøve (serum pepsinogen) som indikerer nivået av magesyre produksjonen blitt vurdert som en screening test basert på det faktum at magekreft er knyttet til en relativ mangel på syre.
Serum pepsinogen kan vise seg å være et nyttig innledende screening test for å indikere hvilke individer bør da ha en gastroskopi, men ville bare være nyttig i et land som Japan med en svært høy forekomst av magekreft.
Bukspyttkjertelkreft
Kreft i bukspyttkjertelen påvirker bare ca 10 personer per 100.000 av den voksne vestlige befolkningen til enhver tid. Dagens tester for kreft i bukspyttkjertelen (blodprøver eller skanner) har en høy falsk-positiv rate på om lag 15 prosent. Så ville utbredt bruk resultere i 15 000 individer feilaktig gitt et positivt resultat for hver 10 pasienter som har kreft i bukspyttkjertelen.
En sak har blitt gjort at screening kan være forsvarlig i svært sjeldne tilfeller av familiær kreft i bukspyttkjertelen. Dette ville kreve svært invasiv endoskopisk pancreatography test (som innebærer teleskopisk undersøkelse og røntgen i bukspyttkjertelen) pluss prøvetaking av bukspyttkjertelen juice, en test som ville bære om en tre prosent risiko for å forårsake akutt betennelse i bukspyttkjertelen (pankreatitt), i seg selv en alvorlig og svært ubehagelig tilstand.
Dette screeningprogrammet er derfor svært eksperimentell i dag.
Leverkreft
Undersøkelse av mennesker etter døden viser at om lag 50 prosent av pasienter med skrumplever har primær leverkreft (hepatocellulær karsinom) på tidspunktet for dødsfallet selv om det forårsaket dødsfallet i bare ca 10 prosent.
Nivået av et protein som kalles alfa fetoprotein øker i blodet til omtrent 70 prosent av de berørte individer. Vanlig praksis er å undersøke protein nivåene med en blodprøve hver sjette måned hos pasienter med cirrhose som er betraktet plass nok til å tåle de større kirurgiske inngrep (vanligvis fjerning av en del av leveren) som ville være nødvendig for en kur.
Screening eller forebygging?
Hver gastrointestinal kreft har en annen screening test, og selv for kolorektal kreft, er potensialet for økt overlevelse i den gjennomsnittlige person som gjennomgår screening ikke veldig stor.
En alternativ strategi for den generelle befolkningen er å vedta et forebyggende tiltak som kan samtidig redusere risikoen for død av flere forhold.
Tiltak kan omfatte endringer i livsstil som høy grønnsaker, lav-fett, dietter og trening regimer som sannsynligvis vil samtidig redusere risikoen for å dø av tykktarmskreft og iskemisk hjertesykdom (koronarsykdom).
Forebyggende behandling er en annen mulighet. Regelmessig aspirin i doser på 300 mg per dag (kliniske studier pågår for å fastslå en forebyggende dose) eller mer har vist seg å omtrent halvere dødelighet av kolorektal kreft, og tilbyr også betydelig beskyttelse mot iskemisk hjertesykdom og slag.
Den kreft-forebyggende virkning er antatt å være forårsaket av aspirin blokkere et enzym (protein som gir raskere kjemiske reaksjoner) kalt cyklooksygenase 2 (COX-2), mens den forebygging av iskemisk hjertesykdom og slag er mediert ved å blokkere COX-1.
Studier foregår, og dem uten er det vanskelig å være sikker på hvorvidt disse gunstige effekter av aspirin kan bli mer enn oppveid av de skadelige effekter, slik som økt risiko for blødning og mage ulcerasjon og blødning i hjernen.
En ny serie av COX-2-hemmere er tilgjengelig, og disse stoffene har ikke de uønskede bivirkninger av aspirin, men vil heller ikke beskytte mot iskemisk hjertesykdom eller slag. Imidlertid er de sannsynligvis vil beskytte mot andre gastrointestinal kreft i tillegg til tarmkreft.
Daglig inntak av en av disse nye stoffene kan vise seg å være minst like effektiv som alle dagens screening strategier satt sammen, men fordelene må alltid veies opp mot risikoen for bivirkninger.
Imidlertid har nyere studier antydet at det i enkelte individer tar disse stoffene kan det nå bli en noe økt risiko for hjerteproblemer knyttet til stoffet. To av disse legemidlene - Vioxx og Bextra - har allerede blitt tatt av markedet, og videre studier er i gang med en annen kalt Celebrex.
Hvis du er opptatt av å ta denne klassen av narkotika, diskutere det med din egen lege.
Andre mennesker også lese:
Tarmkreft: hva som forårsaker tarmkreft?
Magekreft: hvordan er magekreft diagnostisert?
Kreft i spiserøret: Hva er prognosen?
Kreft i bukspyttkjertel: hva er symptomene på cancer i bukspyttkjertelen?